¿Qué tipo de material es el litio de las baterías?
Dependen del litio la mayor parte de las herramientas eléctricas sin cable. Las baterías actuales son de litio por una buena razón. La tecnología de iones de litio permite construir baterías con mayor densidad de energía. En otras palabras, pueden acumular más energía en menos espacio.
Por otro lado, los acumuladores Li-Ion tienen menos efecto memoria que otras celdas recargables de otras clases. Una cualidad que permite aprovechar mejor la energía de la batería. Así, hoy nadie duda que las baterías de litio han llegado para quedarse. Pero ¿qué tipo de material es el litio?

Litio, el metal más ligero que existe
El litio es un metal. No cualquier metal. Es el metal más ligero que existe. De hecho, su densidad es tan baja que flota en el agua. Pesa poco más de medio gramo por cm³ (en concreto: 543 gramos por litro).
En la tabla periódica encontramos el símbolo Li debajo de la letra H. En efecto, el litio (Li) aparece justo debajo del hidrógeno (H), a pesar de no pertenecer a su grupo. En efecto, el H es un gas transparente, mientras que el litio es un metal alcalino.
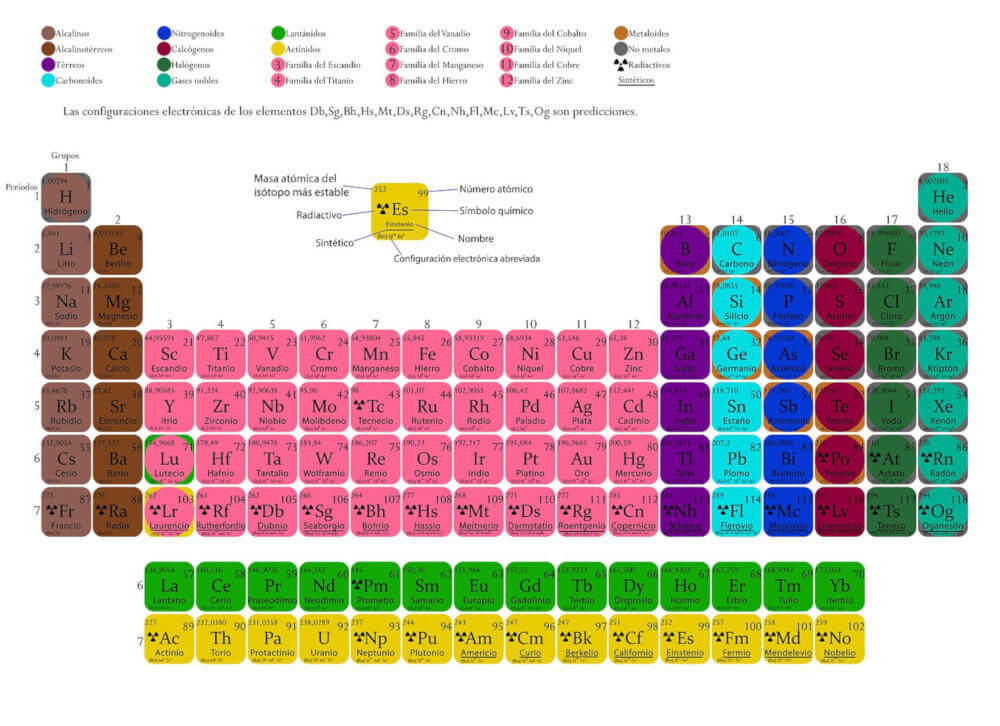
Algunas propiedades del litio como elemento químico
El número atómico del litio es 3, lo que quiere decir que tiene tres protones en su núcleo. Este elemento químico también tiene tres electrones en órbita alrededor del núcleo, donde también residen cuatro protones. El peso atómico del litio es 6.941.
Nota: el peso atómico de un elemento químico es un ratio del promedio de la masa de los átomos del material en una muestra dada con respecto a la constante de masa atómica.
En la naturaleza no se encuentra litio puro. Este metal ligero es sumamente reactivo y cuando reacciona con el agua forma compuestos capaces de neutralizar el poder corrosivo de los ácidos. Esta propiedad la comparte con el resto de metales alcalinos. Que son: sodio, potasio, rubidio, cesio y francio.
Vídeo recomendado del canal Cienciabit de YouTube sobre el litio
▶
Este vídeo está bloqueado para proteger tu privacidad. Haz clic para verlo y aceptar las cookies de YouTube.
El elemento comestible de las baterías
Se desconoce qué función desempeña el litio en el cuerpo humano. Sin embargo, se trata de un metal no le falta a nadie en el organismo. Se ingiere litio al comer, por ejemplo, setas, semillas y frutos secos. ¡Eso no significa que la batería del taladro sin cable sea comestible!
Por cierto, cambiando de tema, desde 2015 cientificos investigan cómo mejorar el rendimiento de las baterías de iones de litio precisamente con hongos. En concreto, con champiñones portobello.
Las plantas absorben Li del suelo. También lo hacen los crustáceos del agua del mar. El agua marina contiene disuelta en su composición litio. De hecho, los océanos contienen cientos de miles de toneladas del alcalino elemento.
Aplicaciones del litio
Industrialmente hoy el litio se utiliza sobre todo para fabricar baterías recargables. La corriente eléctrica de estas baterías no solo alimenta herramientas como sierras, taladros y lijadoras. Pues también las encontramos en ordenadores portátiles, teléfonos móviles o coches eléctricos.
Sin embargo, el metal que flota en agua también sirve para:
- Fabricar los espejos de los telescopios (reduce el deformamiento del vidrio en temperaturas extremas)
- Elaborar grasa lubricantes multipropósito (basada en jabón de hidróxido de litio)
- Absorber humedad del aire (deshumidificadores basados en bromuro y cloruro de litio)
- Tratar enfermedades como el trastorno bipolar (con pequeñas dosis de carbonato de litio)
- Fabricar protesis dentales (en forma de cerámica por su resistencia al desgaste)
- Mejorar la resistencia al calor del vidrio cerámico (disminuye el punto de fusión y mejora el escurrimiento)
- Disminuir el punto de fusión del baño de aluminio (metal ligero que se obtiene por electrólisis), lo que posibilita ahorrar energía y emitir menos flúor al medioambiente
No podemos concluir este artículo sin hacernos una pregunta. ¿De dónde se extrae el litio de las baterías? El más ligero de los metales se extrae de minerales como la petalita (o castorita) y la lepidolita:

Foto de Eurico Zimbres, CC BY 2.5, Wikimedia Commons
Seguridad
Como colofón, el litio y el resto de metales alcalinos liberan calor al entrar en contacto con el agua. Estas reacciones químicas exotérmica pueden llegar a ser muy peligrosas.
Por tanto, antes de manipular tales elementos químicos, conviene por seguridad leer la NTP 237: Reacciones químicas peligrosas con el agua (PDF). Esta Nota Técnica de Prevención la publica el INSST, Instituto Nacional de Seguridad y Salud en el Trabajo.